작성자 : admin작성일 : 2019-08-27 18:45
임상진행 및 리보세라닙의 적응증 현황
임상진행 및 리보세라닙의 적응증 현황
주주 여러분, 리보세라닙의 임상 현황에 대해 설명드리겠습니다.
아래 임상현황은 리보세라닙의 가치와 에이치엘비의 기업 가치를 판단하는 데 있어서 가장 중요한 지표입니다.

1. 위암 3차 : 글로벌 임상 3상종료 후 FDA pre-NDA 미팅(신약허가신청을 위한 사전 미팅)을 신청하였으며, 10월 중순경 FDA와 미팅을 예상합니다.
2. 간암 1차 : 리보세라닙 + 캄렐리주맙 병용, 진행성 간 세포암(Advanced Hepatocellular Carcinoma) 타겟의 글로벌 임상 3상이 진행중입니다.
간암 1차 치료제 시장은 14조 규모에 이릅니다.
3. 선양낭성암종 1차/2차 : 전이성 선양낭성암종((Adenoid Cystic Carcinoma, ACC)에 대한 유효성과 안전성 평가를 위해 약 12개 병원, 환자 55명을 대상으로 오픈라벨/다기관 임상 2상 시험을 美 FDA로부터 승인받았습니다. 2상 후 바로 NDA 신청이 가능합니다.
위 1~3은 임상을 최종 종료하였거나(위암) NDA 전 최종 임상단계에 있습니다.
따라서 우리는 내년 위암 치료제를 시작으로 매년 하나씩의 항암제를 출시하는 것을 목표로 합니다.
4. 대장암 3차 – 리보세라닙+론서프 병용, 대장암 임상 1b/2상을 FDA로 부터 승인 받았습니다. 대장암 3차는 3조 규모의 시장입니다. 임상 1b/2상 시험을 빠른 시간 내에 마무리하고, 약효가 검증되면 글로벌 임상 3상으로 확장할 계획입니다.
5. 위암 2차 : 파클리탁셀 병용, 1/2a상이 진행중이며, 6월 기준으로 38명 모집에 5명 등록했습니다.
6. 고형암(키투루다 병용) : 임상 1/2a상, 요로상피세포암, MSI-H 또는 dMMR 바이오마커를 가진 전이성 고형암, 전이성 위암 등의 유형의 고형암 환자 총 119명으로 진행중입니다.
7. 고형암(옵디보 병용) - 오픈라벨 형태로 고형암 환자 총 38명 대상으로 임상 1상이 진행중입니다.
* 항서제약의 Apatinib(리보세라닙) 임상현황
현재 항서제약에서는 리보세라닙을 22가지 적응증을 대상으로하여 임상 3상을 진행중입니다. 또한 8개 적응증에 대해 캄렐리주맙과 병용임상을 진행중입니다.
(출처: Morgan Stanley).
현재는 위암 치료제로만 판매되고 있으나, 임상 3상의 성공률이 높다는 점 등 을 감안하면, 향후 아파티닙은 10여개의 항암제로 판매될 가능성이 있다는 게 우리의 판단입니다.
신약개발이 특히 어려운 것은, 후보물질의 약효와 안전성 검증을 위한 임상기간이 길고 많은 비용이 소모되는 반면, 성공률이 낮기 때문입니다.
우리는 항서제약이 먼저 간 길 중 가장 안전한 길을 채택하여 글로벌 임상을 진행함으로써 시행착오 비용을 최소화하는 전략을 택할 수 있습니다.
항서제약의 임상이 신약개발의 네비게이터가 되고 있다는 것, 우리 회사만의 가장 큰 장점입니다.
주주 여러분, 리보세라닙의 임상 현황에 대해 설명드리겠습니다.
아래 임상현황은 리보세라닙의 가치와 에이치엘비의 기업 가치를 판단하는 데 있어서 가장 중요한 지표입니다.

1. 위암 3차 : 글로벌 임상 3상종료 후 FDA pre-NDA 미팅(신약허가신청을 위한 사전 미팅)을 신청하였으며, 10월 중순경 FDA와 미팅을 예상합니다.
2. 간암 1차 : 리보세라닙 + 캄렐리주맙 병용, 진행성 간 세포암(Advanced Hepatocellular Carcinoma) 타겟의 글로벌 임상 3상이 진행중입니다.
간암 1차 치료제 시장은 14조 규모에 이릅니다.
3. 선양낭성암종 1차/2차 : 전이성 선양낭성암종((Adenoid Cystic Carcinoma, ACC)에 대한 유효성과 안전성 평가를 위해 약 12개 병원, 환자 55명을 대상으로 오픈라벨/다기관 임상 2상 시험을 美 FDA로부터 승인받았습니다. 2상 후 바로 NDA 신청이 가능합니다.
위 1~3은 임상을 최종 종료하였거나(위암) NDA 전 최종 임상단계에 있습니다.
따라서 우리는 내년 위암 치료제를 시작으로 매년 하나씩의 항암제를 출시하는 것을 목표로 합니다.
4. 대장암 3차 – 리보세라닙+론서프 병용, 대장암 임상 1b/2상을 FDA로 부터 승인 받았습니다. 대장암 3차는 3조 규모의 시장입니다. 임상 1b/2상 시험을 빠른 시간 내에 마무리하고, 약효가 검증되면 글로벌 임상 3상으로 확장할 계획입니다.
5. 위암 2차 : 파클리탁셀 병용, 1/2a상이 진행중이며, 6월 기준으로 38명 모집에 5명 등록했습니다.
6. 고형암(키투루다 병용) : 임상 1/2a상, 요로상피세포암, MSI-H 또는 dMMR 바이오마커를 가진 전이성 고형암, 전이성 위암 등의 유형의 고형암 환자 총 119명으로 진행중입니다.
7. 고형암(옵디보 병용) - 오픈라벨 형태로 고형암 환자 총 38명 대상으로 임상 1상이 진행중입니다.
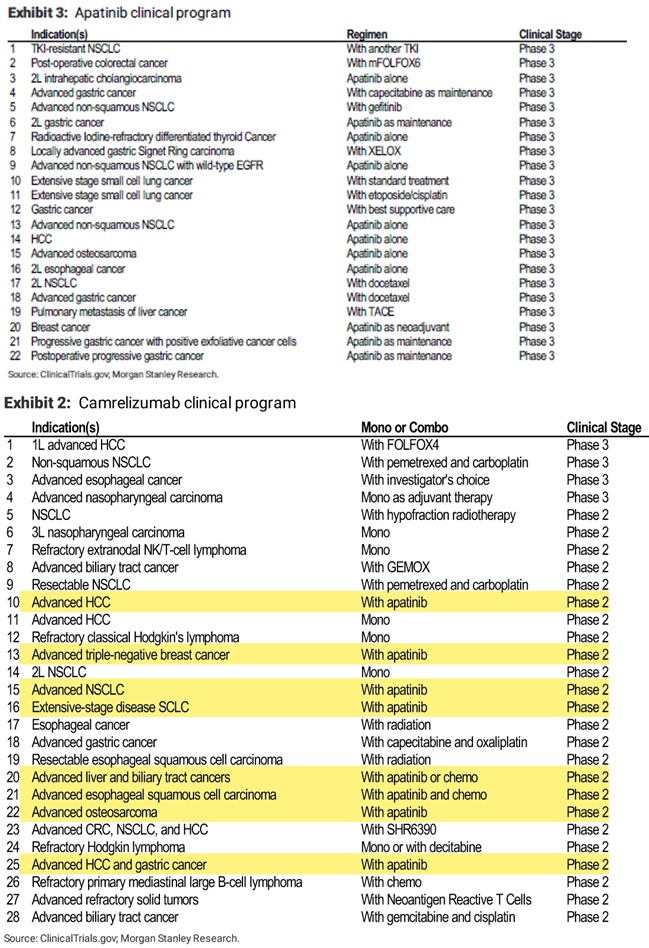
* 항서제약의 Apatinib(리보세라닙) 임상현황
현재 항서제약에서는 리보세라닙을 22가지 적응증을 대상으로하여 임상 3상을 진행중입니다. 또한 8개 적응증에 대해 캄렐리주맙과 병용임상을 진행중입니다.
(출처: Morgan Stanley).
현재는 위암 치료제로만 판매되고 있으나, 임상 3상의 성공률이 높다는 점 등 을 감안하면, 향후 아파티닙은 10여개의 항암제로 판매될 가능성이 있다는 게 우리의 판단입니다.
신약개발이 특히 어려운 것은, 후보물질의 약효와 안전성 검증을 위한 임상기간이 길고 많은 비용이 소모되는 반면, 성공률이 낮기 때문입니다.
우리는 항서제약이 먼저 간 길 중 가장 안전한 길을 채택하여 글로벌 임상을 진행함으로써 시행착오 비용을 최소화하는 전략을 택할 수 있습니다.
항서제약의 임상이 신약개발의 네비게이터가 되고 있다는 것, 우리 회사만의 가장 큰 장점입니다.
에이치엘비, 글로벌 항암제를 시판하는 국내 최초의 회사가 될 것입니다.
