작성자 : admin작성일 : 2020-03-12 14:25
중국 항서제약 리보세라닙적응증 확대
중국 항서제약이 리보세라닙(중국명 아파티닙, 상품명 아이탄)에 대해 단독 또는 병용요법의 개발진행상황을 공지를 통해 밝혔습니다.
지난 2월 27일 리보세라닙의 개발사인 어드벤첸으로부터 중국을 포함한 글로벌 권리를 인수한 에이치엘비는 항서제약의 적응증 확대로 인한 매출증가가 에이치엘비의 로열티 수익증가로 직결되기 때문에 매우 의미있는 정보라고 판단되어 알려드립니다.
항서제약은 리보세라닙 단독요법으로 간암 2차치료제로 중국 국가약품감독관리국(NMPA)에 시판허가를 신청했습니다.
리보세라닙이 단독요법으로 중국에서 넥사바에 실패한 환자 대상으로임상 3상이 진행되었습니다.항서제약이 실시한 임상 3상 결과는 아직 발표되지 않았지만, 여러 연구자에 의해 수행된 임상시험결과에서 매우 의미있는 결과(예, ORR 40.7%)들이 발표되어 결과에 대한 관심이 매우 높습니다.
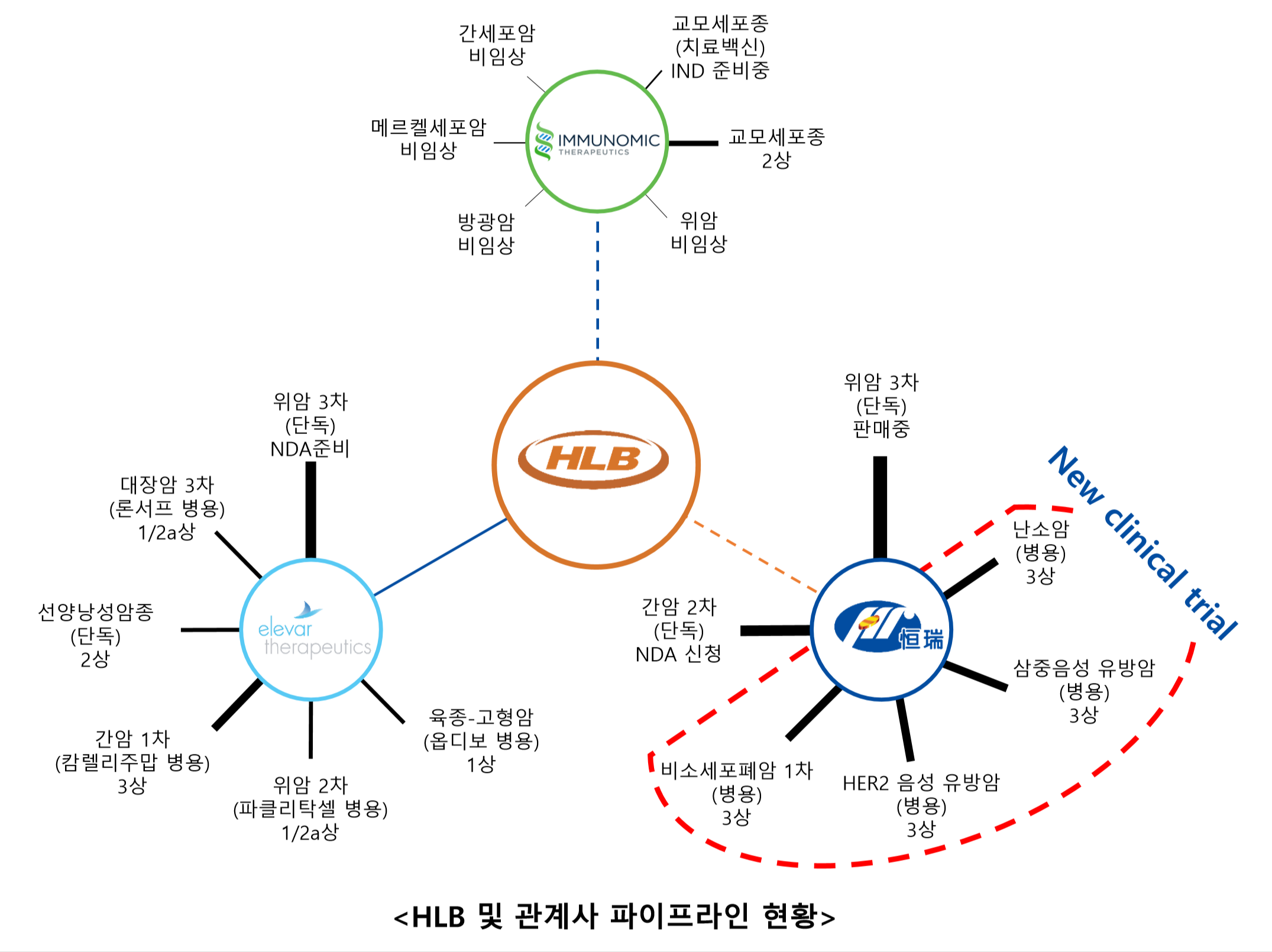
항서제약은 리보세라닙으로 다양한 암종에 대해 70개 이상의 임상시험을 수행하고 있습니다.이번에 4가지 암종에 대해 임상 3상 시험 승인을 받았습니다.
(1) 비소세포폐암 1차 치료제:리보세라닙+ 이레사(Gefitinib) 병용
(2) 3중 음성 유방암(TNBC) 치료제:리보세라닙+ 캄렐리주맙(PD-1 inhibitor) + 파클리탁셀병용
(3) HER2 음성 유방암 치료제: 리보세라닙+ Fluzoparib(PARP inhibitor) 병용
(4) 난소암 치료제:리보세라닙+ Fluzoparib(PARP inhibitor) 병용
2018년 항서제약의 리보세라닙 매출은 약 17억 위안(약 3,000억 원)으로 공식적으로 발표하였습니다.
(1) 간암 2차 치료제 시판 허가 신청으로 중국에서의 리보세라닙 매출 증가가 예상됨에 따라에이치엘비의 로열티 수익이 늘어날 것으로 기대됩니다.
(2) 폐암,유방암,난소암 등 4가지 적응증에 대한 임상 3상 승인은 리보세라닙과의 병용요법으로 진행됩니다.이는 리보세라닙의 다양한 암에서의 높은 효능, 낮은 부작용으로 인해 병용요법에 최적화된 약물이라는 강점이 다시 한번 확인되었습니다.
(3) 항암 치료 개발은 암의 종류에 따라,병용하는 약물에 따라 다양한 변수들이있지만,시간과 비용문제로 인해 모든 것에 대해 임상시험을 진행할 수 없습니다.하지만,에이치엘비의 리보세라닙은 중국에서 다양한 임상시험 결과를 바탕으로 성공적인 임상시험전략을 수립하고 진행할 수 있습니다.
지난 2월 27일 리보세라닙의 개발사인 어드벤첸으로부터 중국을 포함한 글로벌 권리를 인수한 에이치엘비는 항서제약의 적응증 확대로 인한 매출증가가 에이치엘비의 로열티 수익증가로 직결되기 때문에 매우 의미있는 정보라고 판단되어 알려드립니다.
1. 간암 2차 치료제 시판허가 신청
항서제약은 리보세라닙 단독요법으로 간암 2차치료제로 중국 국가약품감독관리국(NMPA)에 시판허가를 신청했습니다.
리보세라닙이 단독요법으로 중국에서 넥사바에 실패한 환자 대상으로임상 3상이 진행되었습니다.항서제약이 실시한 임상 3상 결과는 아직 발표되지 않았지만, 여러 연구자에 의해 수행된 임상시험결과에서 매우 의미있는 결과(예, ORR 40.7%)들이 발표되어 결과에 대한 관심이 매우 높습니다.
2. 임상 3상 승인
항서제약은 리보세라닙으로 다양한 암종에 대해 70개 이상의 임상시험을 수행하고 있습니다.이번에 4가지 암종에 대해 임상 3상 시험 승인을 받았습니다.
(1) 비소세포폐암 1차 치료제:리보세라닙+ 이레사(Gefitinib) 병용
(2) 3중 음성 유방암(TNBC) 치료제:리보세라닙+ 캄렐리주맙(PD-1 inhibitor) + 파클리탁셀병용
(3) HER2 음성 유방암 치료제: 리보세라닙+ Fluzoparib(PARP inhibitor) 병용
(4) 난소암 치료제:리보세라닙+ Fluzoparib(PARP inhibitor) 병용
3. 리보세라닙 중국 판매현황
2018년 항서제약의 리보세라닙 매출은 약 17억 위안(약 3,000억 원)으로 공식적으로 발표하였습니다.
4. 리보세라닙의 가치 확장
(1) 간암 2차 치료제 시판 허가 신청으로 중국에서의 리보세라닙 매출 증가가 예상됨에 따라에이치엘비의 로열티 수익이 늘어날 것으로 기대됩니다.
(2) 폐암,유방암,난소암 등 4가지 적응증에 대한 임상 3상 승인은 리보세라닙과의 병용요법으로 진행됩니다.이는 리보세라닙의 다양한 암에서의 높은 효능, 낮은 부작용으로 인해 병용요법에 최적화된 약물이라는 강점이 다시 한번 확인되었습니다.
(3) 항암 치료 개발은 암의 종류에 따라,병용하는 약물에 따라 다양한 변수들이있지만,시간과 비용문제로 인해 모든 것에 대해 임상시험을 진행할 수 없습니다.하지만,에이치엘비의 리보세라닙은 중국에서 다양한 임상시험 결과를 바탕으로 성공적인 임상시험전략을 수립하고 진행할 수 있습니다.
