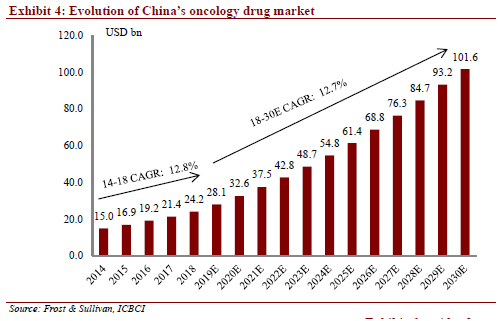
중국 항암제 시장 전망 및 항서제약과의 협업
따라서 중국의 로열티는 항서제약, 중국 외 글로벌 로열티는 엘레바로부터 받게 됩니다.
오늘은 이해를 돕기 위해 중국의 항암제 시장 현황과 항서제약의 리보세라닙 개발 현황에 대해 말씀드립니다.
중국 항암제 시장 전망 및 항서제약과의 협업
중국 항암제 시장
2020년 2월 17일자 ICBC 보고서에 나온 Frost & Sullivan 리서치에 따르면,
- 중국항암제 시장은 최근 4년간(2014~2018년) 연평균 12.8% 성장했고, 2030년까지 연 12.7% 성장을 예상하고 있습니다.
- 매출은 2018년도 USD 24.2bn (29조원)에서 2030년 USD 101.6bn (122조원)으로 예측하고있습니다.
2020년 2월 17일자 ICBC 증권사 보고서에 따르면, 고성장하는 항암제시장에서 항서제약이 중국 항암제 시장의 1등으로써 제일 큰 수혜자라고 예상하고 있습니다.
중국의 항암제 시장이 고성장하는 주요 원인은 1) 고령화, 2) 표적항암제와 면역항암제 시장의 성장입니다.
“China Insights Consultancy(CIC)”에서는 표적항암제와 면역항암제가 전체 시장의 현재 19.2%에서 2030년에 54%까지 성장할 것으로 예상하고있습니다.
주목해야할 리보세라닙의 잠재성 - 항서제약과의 협업
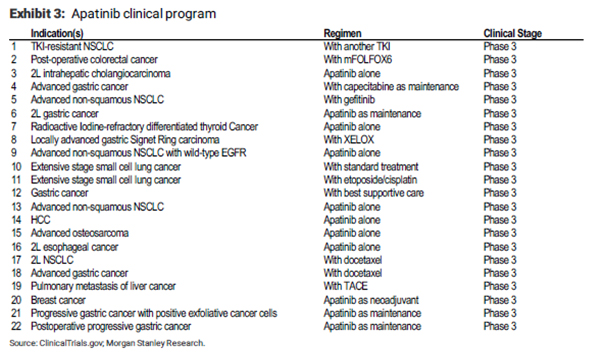
항서제약에서는 리보세라닙으로22가지 적응증으로 임상 3상이 진행중입니다.(아래 표 참조)
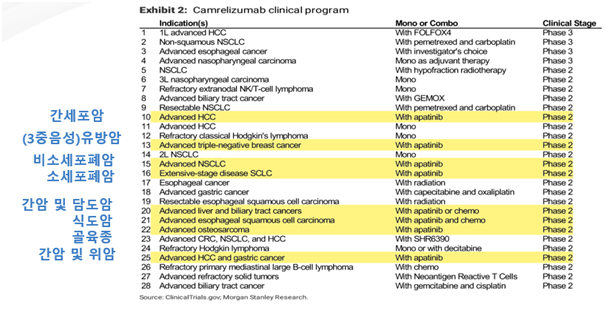
또한 캄렐리주맙과리보세라닙 병용으로 Elevar와 현재 진행중인 글로벌 간암 1차 3상진행뿐 아니라,추가로 7개의 적응증에 대하여 병용임상을 진행중입니다.
(아래 표 참조)
즉 리보세라닙은,
1) 중국에서 22개 적응증 대상 임상 3상 진행중
- 임상 3상이 진행중인 대상 적응증:간암,위암,비소세포폐암, 난소암,위식도암,소세포폐암 등
- 폐암과 간암 임상은 3상임상종료.
2) 캄렐리주맙과 병용으로 7개 적응증대상임상3상 또는 2상 진행중
- 임상 3상이 진행중인 대상 적응증:위암
- 임상 2상이 진행중인 대상 적응증:육종,비세포폐암,소세포폐암,대장암 등
3) 캄렐리주맙과 병용으로 간암 1차 치료제 글로벌 3상 진행중(엘레바와 공동진행)에 있습니다
위 3)은 기존에 중국에서 임상 2상 진행한 것을 엘레바와협업하에,글로벌 3상을 승인받은 것이며,이러한 사례가 추가될 가능성은 충분합니다.
- 향후 항서제약과의 협업이 만들어 낼 가치는 대단히 큽니다
- 바이오 기업에게 있어서 신약의 과정은 시간과 비용이 소요됩니다.그리고 실패의 위험도 상존합니다.
- 다행스럽게도 항서제약이 리보세라닙에 관해 수년간 시간과 비용을 들여 해 온 임상들이 상당히 많고,그중 다수가 3상으로 성과를 목전에 두고 있습니다.그 결과물들이 우리 에이치엘비의 가치로 확장될 수 있도록 할 것입니다
- 또한 글로벌 제약 바이오기업과 신약 리보세라닙과 기업의 잠재적 가치 확장을 위한 오픈 이노베이션이 지속적인 성과로 이어질 수 있도록 최선을 다할 것입니다.